Minden nagy bulinak szomorú a vége…
Jó buli ez a click kémia, de mint minden teleshopos cuccnak, csak vannak hátulütői?!
Mi választja el a click
kémiát attól, hogy a szent grál legyen?
Mik a határai?
Mindenek előtt, ha valaki az azidokkal foglalkozó cikket olvas
(leszámítva a mi két cikkünket :D), általában csupa nagybetűvel, félkövéren
kiszúrja a szemét, hogy az azidokkal vigyázni kell, mert felrobbanhatnak.
Láttatok már légzsákot? Az is azid. A szerves azidok is robbanásveszélyesek
LEHETNEK. Hogy mikor azok ténylegesen, arra létezik néhány ökölszabály. A „hármas szabály” a nitrogén- és
szénatomok számának hányadosával operál, pontosabban az (oxigénatomok száma +
szénatomok száma)/nitrogénatomok száma hányados nagysága alapján rangsorolja az
azidokat:
- ha ez nagyobb mint három, akkor az azid stabilnak tekinthető. A kilenc szénatomos nonil-azid a legkisebb alkil-azid, ami izolálható, és tárolható tiszta formában is (20 g mennyiségig). Erre a vegyületre a hányados pont három,
- ha a hányados egy és három közé esik, akkor előállítható ugyan az azid és izolálható is, de csak hűtve szabad tárolni, maximum 5 grammos tételben, és legfeljebb 1 M koncentrációjú oldatban,
- egy alatti hányadossal jellemezhető azidokat nem szabad izolálni. Előállíhatóak, mint intermedierek és minor komponensként használhatóak egy reakcióban, de legfeljebb egy grammos mennyiségben.
Alternatívát nyújt a „hatos
szabály”. Eszerint hat szén (vagy hasonló méretű hetero)atomnak kell esnie
egy energiadús (és ezért potenciálisan veszélyes) funkciós csoportra (azid,
diazo, nitro stb.), hogy megfelelő óvatosság mellett biztonságosan kezelhető
vegyületeket kapjunk.
A szerves azidok toxicitására általánosságban nincs adat,
ezért érdemes a nátrium-azidból kiindulva mérgezőnek tekinteni őket.
Ezeken a potenciális veszélyeken sokat tompíthat, ha az
azidot in situ állítjuk elő.
Lehetőség van pl. a click reakciót úgy megvalósítani, hogy az acetilén mellé
nem az azidot tesszük a lombikba reakciópartnerként, hanem a megfelelő
halogénvegyületetet és nátrium-azidot. A lombikban "előbb" lejátszódik a
nukleofil szubsztitúció, és a keletkező kis mennyiségű szerves azid gyorsan el
is reagál, a click reakcióban, nem halmozódik fel.
Aztán a másik baj a click reakcióval, hogy egy
cikloaddícióról van szó. Vagyis a dienofil nem lehet túlzottan elektronban
gazdag. A dién nem lehet túlzottan elektronban szegény. A „dién” a Huisgen
cikloaddícióban az azid, míg a dienofil az acetilén. Szerencsére a biológiai
rendszerekben, illetve a gyógyszermolekulákban ritkán fordulnak elő olyan funkciós
csoportok, amik ezt előidéznék.
Egy másik útonálló, aki a missziót meghiúsíthatja, az
acetilén homokapcsolása, vagyis két acetilénmolekula egymással való reakciója.
Ez három mechanizmus szerint is lehetséges, három különböző terméket
szolgáltatva. Ami közös bennük, hogy rézkatalizáltak, és csökkentik a click
reakció kihozatalát.
Első Glazer. Ezt a Cu(I) katalizálja és oxigén jelenléte is
szükséges, hogy végbemenjen.
Második Straus. Egy essel. Szintén Cu(I) katalizált, levegőn
és inert atmoszférán is lejátszódik.
Harmadik: Eglinton.
Őt a Cu(II) ionok katalizálják.
Ami még közös a homokapcsolási mellékreakciókban, hogy a
kisméretű bázis kedvez a lejátszódásuknak, tehát sztérikusan zsúfolt bázis
használatával elkerülhetőek vagy háttérbe szoríthatóak. Bázist egyébként az
alkin-Cu(I) komplex deprotonálódásának megkönnyítésére szokás a click
reakcióhoz adni, amire főleg nembázikus oldószerekben lehet szükség. Így
keletkezik a Cu-acetilid, aminek az aziddal kell reagálnia katalitikus
körfolyamat következő lépésében.
Aztán problematikus lehet a Cu-katalízis. Ugyan a réz biogén
elem (lásd erről korábbi bejegyzésemet), hiánybetegsége is van, a hosszadalmas
rézzel való érintkezést összefüggésbe hozták olyan komoly betegségekkel is, mint
Alzheimer-kór, vesebetegségek, idegrendszeri rendellenességek. Ennek hátterében
az áll, hogy a réz könnyen vesz vesz egyelektron felvételi-leadási reakciókban,
így toxikus mellékreakciókat
katalizálhat in vivo.
Aztán bár az 1,2,3-triazol csoportot régóta ismeri a
tudomány, még alig tudunk valamit az élő szervezetben való sorsáról, csupán
néhány származékot vizsgáltak részletesebben, amiből általános információk
egyelőre nem vonhatóak le.
És végül probléma, hogy sok click prekurzor (azid ill.
acetilén) nem elérhető kereskedelmi forgalomban, elő kell őket állítani, ami
pl. egy molekulakönyvtárat szintetizáló gyógyszerkémikus számára sok
pluszmunkát jelent. Ez a probléma valószínűleg csak átmeneti, a vegyszergyártók
is felismerték a click reakcióban rejlő potenciált.
Mindezekkel a limitációkkal együtt azonban azt gondoljuk, hogy
a click reakcióval Sharpless kijelölt egy olyan útirányt, amin járni érdemes.


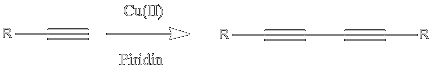
Nincsenek megjegyzések:
Megjegyzés küldése